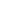8月14日,國家藥監局發布最新藥品批準證明文件。
本批6品種、9品規藥品補充審批獲批,通過一致性評價。
其中,上海禾豐制藥兩個品種過評,分別是重酒石酸間羥胺注射液、鹽酸去氧腎上腺素注射液,過評企業均達4家;注射用氨芐西林鈉舒巴坦鈉有2家企業同日過評,分別是山東道齊生物和杭州沐源生物,過評企業已滿5家。
過評品種如下:
上海禾豐制藥-重酒石酸間羥胺注射液
重酒石酸間羥胺是一種升血壓藥,用于防治椎管內阻滯麻醉時發生的急性低血壓;由于出血、藥物過敏、手術并發癥及腦外傷或腦腫瘤合并休克而發生的低血壓,本品可用于輔助性對癥治療;也可用于心源性休克或敗血癥所致的低血壓。
重酒石酸間羥胺注射液為2018版國家基藥、2022版國家醫保甲類藥,還曾多次出現在各省市的短缺藥名單中,可見其產品地位十分重要。米內網數據顯示,2021年在中國公立醫療機構終端銷售額已超過9億元,北京市永康藥業占領了大部分份額。
目前,國內有13家企業擁有重酒石酸間羥胺注射液的生產批文。其中4家企業過評,除了此次的上海禾豐制藥,天津金耀藥業(首家)、成都欣捷、南京澤恒醫藥在此前已經相繼過評。另外,浙江醫藥和北京市永康藥業的一致性評價申請也在審評審批階段。
上海禾豐制藥-鹽酸去氧腎上腺素注射液
鹽酸去氧腎上腺素注射液是一種血管升壓藥,可增加外周血管阻力,升高收縮壓和舒張壓,適用于治療休克及麻醉時維持血壓,也用于控制陣發性室上性心動過速。作為單純的ɑ1腎上腺素能受體激動劑,去氧腎上腺素無直接興奮心臟作用,能反射性地減慢心率。血管升壓藥主要分為縮血管藥和正性肌力藥,去氧腎上腺素為縮血管藥,較同類去甲腎上腺素作用更持久。可廣泛應用于麻醉手術及急搶,是2022版國家醫保甲類藥物。
鹽酸去氧腎上腺素注射液由Avaedl Legacy研發,1954年首次在美國上市。
在2022年以前,國內僅有上海禾豐制藥一家獲批生產銷售鹽酸去氧腎上腺素注射液。2022年5月,成都苑東的產品獲批并首家過評;2023年3月,合肥億帆生物制藥和廣東中潤藥物的產品也獲批并過評。目前過評企業達4家。
另外,還有9家企業提交了鹽酸去氧腎上腺素注射液的上市申請,處于審評審批階段,包括石四藥、倍特藥業等。
根據米內網數據,去氧腎上腺素2022年市場規模約6000萬元。
注射用氨芐西林鈉舒巴坦鈉
注射用氨芐西林鈉舒巴坦鈉是青霉素復合制劑,原研為輝瑞,適用于治療由敏感細菌所引起的感染。
氨芐西林是β-內酰胺類抗生素,屬氨基青霉素類,對腸球菌抗菌活性很強,易被β-內酰胺酶水解。作用特點是廣譜,不耐青霉素酶。舒巴坦是β-內酰胺酶抑制劑,對不動桿菌有較好的抗菌活性;可保護β-內酰胺類抗生素不受β-內酰胺酶水解。舒巴坦與氨芐西林聯合使用可大大提高后者的抗菌作用。
從2020年開始,氨芐西林鈉舒巴坦鈉市場有所突破,目前呈階梯式上漲趨勢。根據米內網數據,2022年氨芐西林舒巴坦中國公立醫療機構終端銷售額2022年銷售額近5億元,2021年、2022年分別同比增長119.99、145.78%。
目前國內已有33家廠商(包括原研)獲批生產注射用氨芐西林鈉舒巴坦鈉,其中海南通用三洋藥業(首家)、湖南科倫制藥和成都倍特藥在今年已經陸續過評,加上此次的山東道齊和杭州沐源,目前過評企業已滿5家。另外還有5家企業提交了一致性評價申請,包括山東魯抗醫藥、蘇州二葉制藥等。
注:文章來源于網絡,如有侵權,請聯系刪除




 全部商品分類
全部商品分類